LA EMPRESA farmacéutica estadounidense Eli Lilly afirma que su terapia con anticuerpos monoclonales ayudó a prevenir la infección de COVID-19 en un ensayo clínico.
Pero, ¿qué es la terapia con anticuerpos monoclonales?
Los anticuerpos son proteínas que produce nuestro sistema inmune para combatir distintos microorganismos como los virus, entre ellos, el SARS-CoV-2, causante del COVID-19. Los anticuerpos monoclonales se producen en laboratorios, pero funcionan prácticamente igual que los que se generan naturalmente en nuestro cuerpo.
Actualmente, se han creado terapias en las que se utilizan anticuerpos desarrollados en el laboratorio para tratar a las personas que han dado positivo en la prueba de COVID-19 y presentan síntomas de leves a moderados.
A la fecha, la Administración de Alimentos y Medicamentos de Estados Unidos (FDA, por sus siglas en inglés) ha autorizado dos de esos tratamientos para su uso de emergencia: casirivimab e imdevimab administrados en conjunto, y bamlanivimab, administrado individualmente.
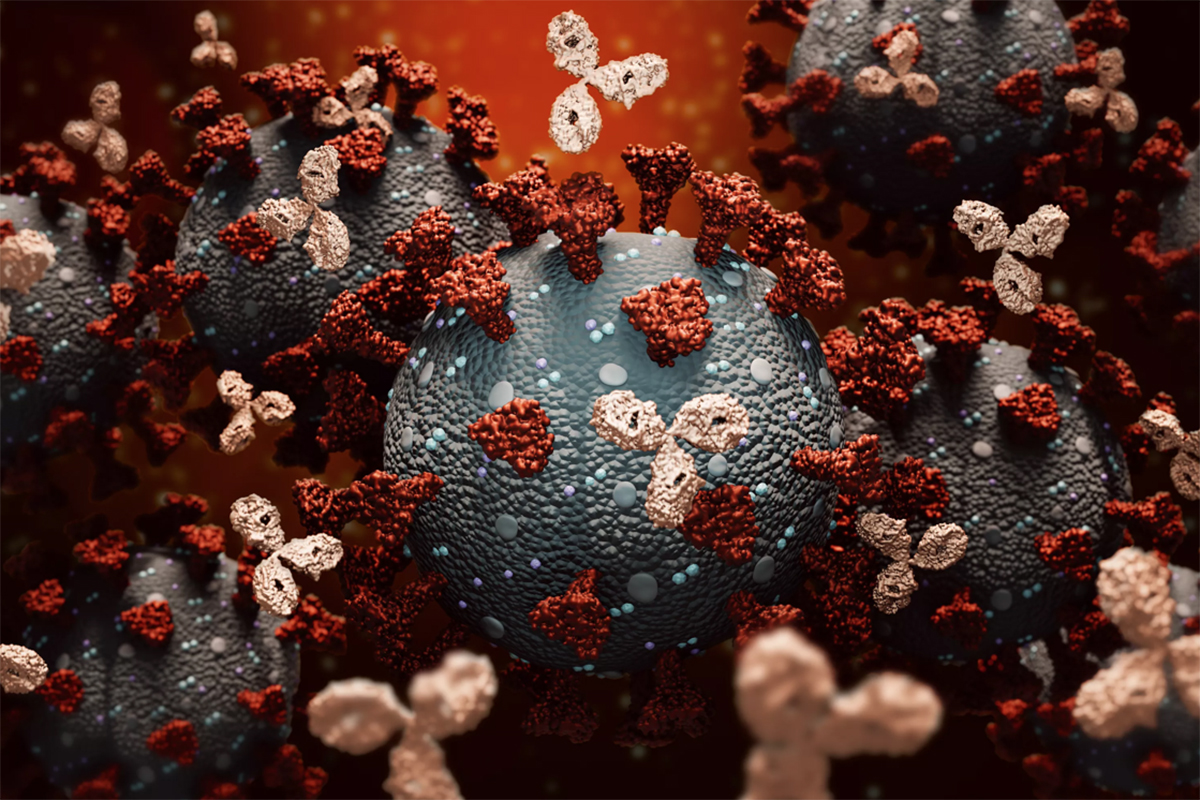
Estos anticuerpos monoclonales atacan a la proteína “spike” del virus SARS-CoV-2, que este utiliza para enlazarse y entrar en las células humanas. Al enlazarse a la proteína “spike”, los anticuerpos bloquean la entrada del virus a dichas células.
Lee: La protección de anticuerpos tras una infección de COVID-19 “disminuye con bastante rapidez”
Aún se investiga la seguridad y efectividad del tratamiento con bamlanivimab, pero en ensayos clínicos previos se ha mostrado que reduce los índices de hospitalización o de uso de salas de emergencia relacionadas con el COVID-19 en pacientes con un riesgo alto de agravación.
Sin embargo, el bamlanivimab no está autorizado para tratar a los pacientes que ya están hospitalizados por COVID-19 o requieren oxígeno como resultado de esta enfermedad, de acuerdo con la FDA.
El reciente anuncio de Eli Lilly se refiere a un estudio que la empresa realizó para examinar el tratamiento con bamlanivimab que estaba encargada de desarrollar.
En el ensayo de fase III, la empresa señaló que el bamlanivimab “disminuyó de manera importante” el riesgo de contraer COVID-19 sintomático entre los residentes y el personal de instituciones de atención a la salud a largo plazo. Esta es la primera vez que se muestra que una terapia con anticuerpos monoclonales previene la infección de COVID-19 en lugar de simplemente tratar la enfermedad.
El jueves pasado, Lilly publicó un comunicado en el que detalla los resultados del estudio, aunque la empresa aún no los publica en ninguna revista clínica revisada por pares. La farmacéutica señaló que planea enviar pronto a una revista científica los resultados del ensayo, que fue supervisado por un consejo independiente de vigilancia de datos y seguridad.
“Estamos excepcionalmente complacidos con estos resultados positivos, que muestran que el bamlanivimab fue capaz de ayudar a prevenir el COVID-19, disminuyendo de manera sustancial la enfermedad sintomática entre residentes de casas de retiro para ancianos, que son algunos de los miembros más vulnerables de nuestra sociedad”, afirmó Daniel Skovronsky, director científico de Lilly y presidente de Lilly Research Laboratories.
“Esos datos proporcionan importantes evidencias clínicas adicionales en relación con el uso del bamlanivimab para combatir el COVID-19 y aumentan nuestra convicción de que los anticuerpos monoclonales como el bamlanivimab pueden tener una función muy importante para cambiar el rumbo de esta pandemia”.
DETALLES SOBRE EL ESTUDIO
Skovronsky añadió que la empresa espera analizar con los organismos reguladores la ampliación de la autorización del uso de emergencia del bamlanivimab para que este tratamiento pueda ser usado para prevenir la propagación del COVID-19 en las casas de retiro para adultos mayores.
Para este estudio, que se realizó en colaboración con el Instituto Nacional de Alergias y Enfermedades Infecciosas de Estados Unidos, Lilly reclutó 1,097 participantes que trabajaban y vivían en casas de retiro para adultos mayores. Al inicio del estudio, 132 de esas personas dieron positivo en la prueba de SARS-CoV-2: 41 residentes y 91 miembros del personal.
De los 965 participantes que dieron negativo a la prueba del virus al inicio del estudio, 299 eran residentes y 666 eran miembros del personal.
Entérate: COVID-19: Roche se asocia con Moderna para incluir prueba de anticuerpos en ensayos de vacuna
Todos los participantes fueron divididos aleatoriamente para recibir 4,200 miligramos de bamlanivimab por vía intravenosa, una dosis seis veces mayor que la autorizada previamente, o un placebo.
Después de ocho semanas, los investigadores observaron una frecuencia significativamente menor de COVID-19 en las personas que recibieron el bamlanivimab, en comparación con quienes recibieron el placebo.
Además, Eli Lilly indicó que las personas que formaban parte del grupo de 299 residentes de las casas de retiro que dieron negativo al inicio del estudio y que recibieron el bamlanivimab presentaron un riesgo 80 por ciento menor de contraer COVID-19, comparadas con los residentes que recibieron el placebo.
Te puede interesar: Bebé nace con anticuerpos contra el COVID-19
Durante la realización del estudio, cuatro de esos 299 residentes murieron por COVID-19, todos los cuales formaban parte del grupo que recibió el placebo. Entre los 41 residentes que dieron positivo a la prueba de COVID-19 al inicio del estudio, también se presentaron cuatro fallecimientos; todos ellos formaban parte del grupo que recibió el placebo.
Myron Cohen, uno de los investigadores principales del estudio y director del Instituto de Salud Global y Enfermedades Infecciosas de la Universidad de Carolina del Norte, en Chapel Hill, declaró: “La actividad antiviral observada en el tratamiento con bamlanivimab destaca la importancia de la intervención temprana para ayudar a contrarrestar el devastador impacto que el virus ha tenido en esta población vulnerable y en otros pacientes de alto riesgo”.
Skovronsky declaró a STAT que el tratamiento no se debe considerar como una alternativa a las vacunas, que son “más efectivas” y que probablemente darán una protección “más duradera”.
“Se debería usar cuando es demasiado tarde, cuando se produce un brote y las personas están expuestas y no hay tiempo para que la vacuna tenga efecto”, dijo.
—∞—
Publicado en cooperación con Newsweek / Published in cooperation with Newsweek