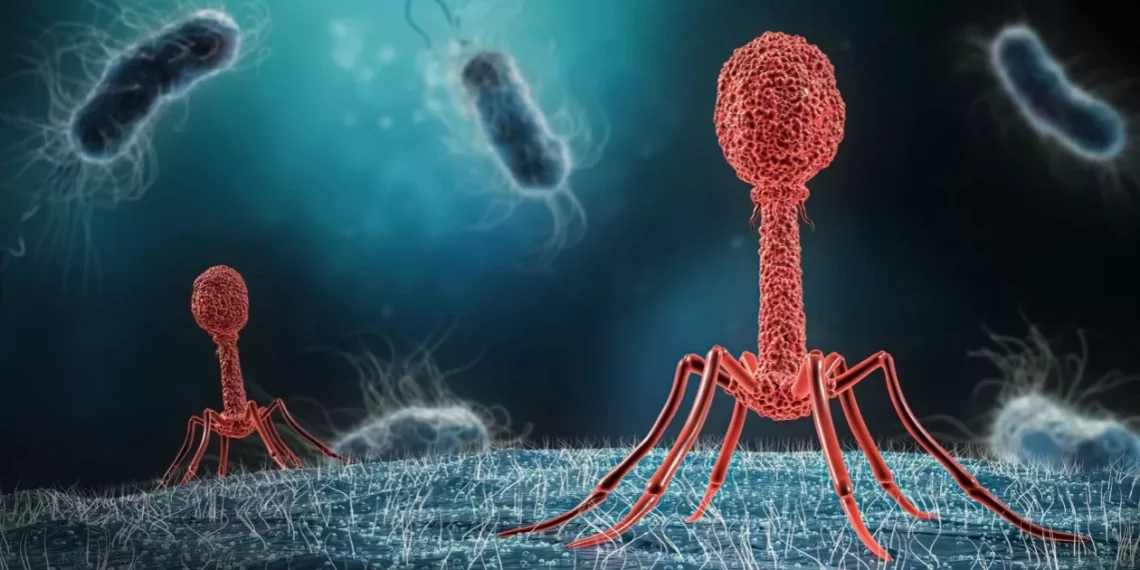
Una de las amenazas sanitarias más graves de nuestra era es el inminente surgimiento de las bacterias resistentes a los antibióticos, las llamadas superbacterias. Y es que lenta, pero ineludiblemente, los gérmenes que combatimos con medicamentos han evolucionado a lo largo de décadas para volverse resistentes a los antibióticos.
No obstante, este problema no solo es enorme, sino que está expandiéndose a todo el mundo conforme las infecciones bacterianas se hacen resistentes a nuestro arsenal farmacológico.
Una de las posibles soluciones al problema podría fundamentarse en un aliado de lo más improbable: los virus. Según la Organización Mundial de la Salud (OMS), los patógenos responsables de infecciones como neumonía, tuberculosis, septicemia y gonorrea están adquiriendo rápida resistencia a los antibióticos que solíamos utilizar para combatirlos.
Tomemos el caso de las cepas de Staphylococcus aureusidentificadas en Estados Unidos: muchas ya son resistentes a la penicilina, mientras que otras empiezan a adquirir resistencia a la meticilina, causando lo que hoy se conoce como infecciones SARM (siglas de Staphylococcus aureusresistente a la meticilina).
“Las superbacterias son gérmenes que han evolucionado la capacidad de resistir [o de volverse resistentes a] los antibióticos y demás medicamentos que usamos para tratar infecciones. Este fenómeno recibe el nombre de resistencia antimicrobiana, designado con las siglas RAM”, explica a Newsweek el Dr. Jeremy Barr, profesor de microbiología ambiental en la Universidad de Monash, Australia.
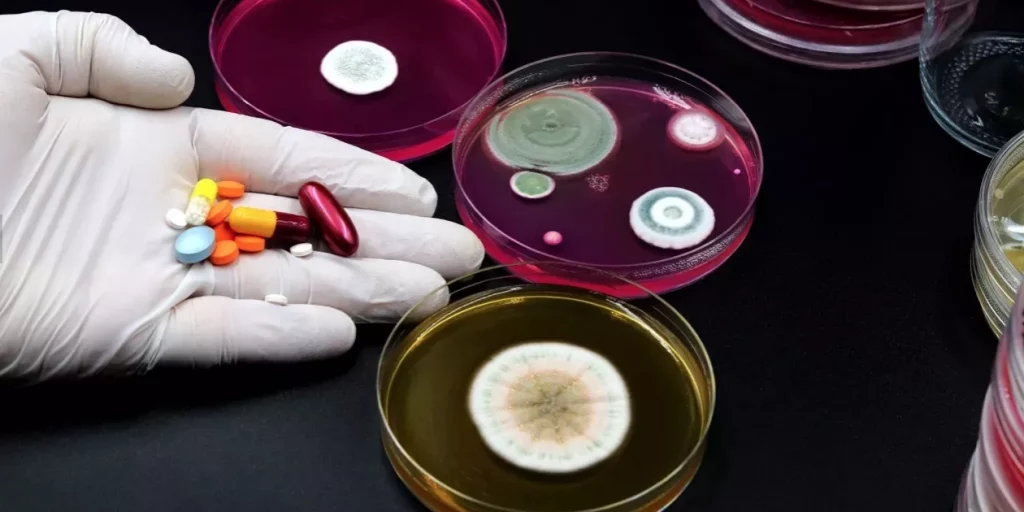
BACTERIAS RESISTENTES A ANTIBIÓTICOS
“La resistencia antimicrobiana es un proceso natural. De hecho, hemos descubierto bacterias resistentes a los antibióticos en especímenes que tienen cientos de miles de años de antigüedad”, agrega el científico. “Por lo que respecta a las superbacterias, el abuso y la dependencia generalizada de los antibióticos ha resultado en el desarrollo o la selección de cepas que muestran cada vez mayor resistencia a esa familia de fármacos. En pocas palabras, cuanto más utilicemos un antibiótico, más pronto aparecerá una superbacteria”.
Los Centros para el Control y Prevención de Enfermedades afirma que Estados Unidos registra más de 2.8 millones de infecciones de resistencia antimicrobiana cada año, las cuales resultan en cerca de 35,000 defunciones anuales. Entre tanto, las proyecciones para RAM apuntan a que, hacia 2050, las infecciones por bacterias resistentes ocasionarán 10 millones de muertes anuales en todo el mundo.
“Hay numerosos informes de infecciones debidas a superbacterias específicas que se han vuelto resistentes a todos los antibióticos clínicamente relevantes”, agrega Barr. “Así que ahora tenemos que dar marcha atrás y usar antibióticos de primera generación como último recurso, o bien, recurrir a otros fármacos que conllevan problemas de toxicidad, porque ningún otro medicamento combate esas infecciones”.
¿Qué podemos hacer para contener la marejada de infecciones bacterianas que son cada vez más resistentes a los tratamientos utilizados para combatirlas? Muchos científicos apuestan a que la solución son los virus que matan bacterias: los llamados bacteriófagos o, simplemente, “fagos”. Y la razón es que los bacteriófagos se cuentan entre los organismos más diversos y abundantes de la tierra.
MÁS FAGOS QUE CÉLULAS HUMANAS
“Hay más fagos en el planeta que estrellas en el universo”, asegura Barr. “Hay más fagos en tu cuerpo que células humanas”. Gracias a que los fagos son depredadores naturales de las bacterias, podemos usarlos para combatir infecciones bacterianas.
“Son una alternativa que podemos utilizar por sí sola o en combinación con antibióticos convencionales”, dice a Newsweek el Dr. Andrew Millard, profesor asociado de genética y biología genómica en la Universidad de Leicester, Reino Unido.
“Como en todo, hay ventajas y desventajas. Por ejemplo, los fagos suelen atacar un tipo específico de bacteria; pero, a cambio, no arrasan con la flora intestinal como hacen los antibióticos. Digamos que los antibióticos son como bombas, mientras, los fagos lanzan ataques de precisión contra las bacterias que causan enfermedad”, apunta Millard.
En otras palabras, una de las limitaciones principales del uso de fagos es también uno de sus beneficios principales, ya que solo atacan un tipo de bacterias. “A diferencia de los antibióticos, que matan distintos tipos de bacterias al mismo tiempo, los fagos tienen especificidad bacteriana”, interpone Barr. “Esto significa que, para tratar una infección con fagos —lo que llamamos fagoterapia o terapia con fagos—, primero debemos encontrar el virus que ataca la bacteria específica del paciente”.
“Una gran ventaja es que la variedad de fagos es casi ilimitada, así que no agotaremos este recurso como hemos hecho con los antibióticos. Además, debido a que los bacteriófagos son muy específicos, no provocan los efectos colaterales de los antibióticos; por ejemplo, no destruyen el microbioma intestinal”, añade el profesor de microbiología.
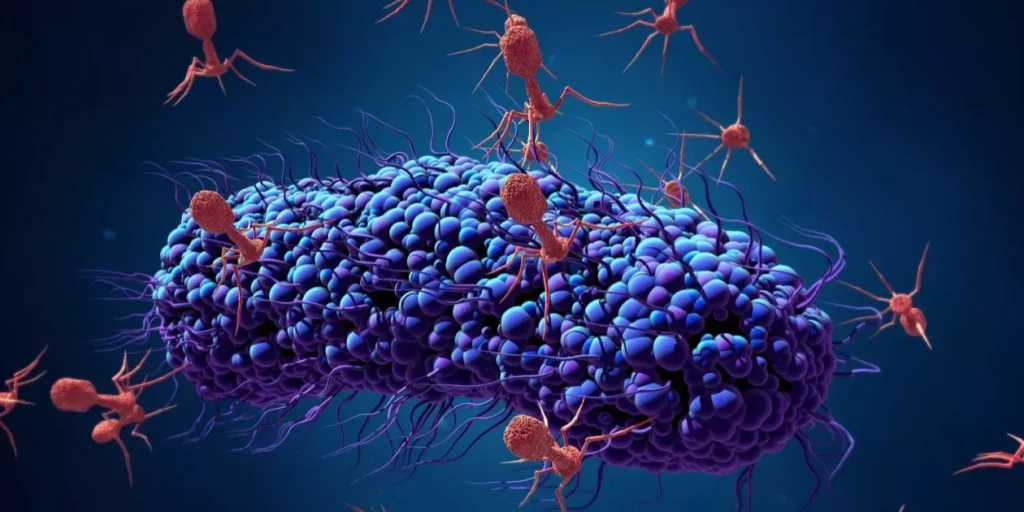
EL ABUSO DE ANTIBIÓTICOS
Otro beneficio es que los fagos pueden desplazar el uso de antibióticos en sectores ajenos al ámbito médico; por ejemplo, en la industria agrícola. “La agricultura hace uso intensivo de los antibióticos; de hecho, esa industria consume gran parte de la producción farmacológica”, revela Barr.
“El problema es que el abuso de antibióticos en el sector agrícola propicia el desarrollo de resistencia antimicrobiana [RAM], la cual puede transferirse a las bacterias que infectan a las personas. Por ello, si reducimos el uso de antibióticos en otros sectores y promovemos la fagoterapia en humanos, podríamos resolver el problema de las superbacterias mediante una estrategia denominada ‘One Health’ o ‘Una sola salud’”.
Aun cuando la terapia con fagos se antoja la solución idónea, persiste un problema: las bacterias también pueden desarrollar resistencia a los fagos. “Las bacterias poseen varios mecanismos para combatir los bacteriófagos y volverse resistentes; es un proceso completamente natural que ha ocurrido desde hace millones de años. Y, por su parte, los fagos también evolucionan para sobreponerse a la resistencia que adquieren las bacterias”, prosigue Barr.
“En otras palabras, se trata de una carrera armamentista evolutiva que no tiene final. De manera que sí, las bacterias llegan a volverse resistentes a los fagos”, añade el experto.
Pero no todo está perdido, porque existe la posibilidad de mitigar la resistencia bacteriana a los fagos. “Las combinaciones de bacteriófagos —los cocteles de fagos— ayudan a prevenir ese problema, porque las bacterias pueden desarrollar resistencia a uno, mas no a todos los fagos”, asegura Millard, el genetista de la Universidad de Leicester.
FAGOS VS. SUPERBACTERIAS
“Hay muchas variedades de fagos, de modo que, si hiciéramos combinaciones con diferentes tipos de virus, podríamos impedir la resistencia bacteriana. Y los ‘cocteles de fagos’ son justamente el objetivo de numerosos proyectos en curso”, añade.
Por otra parte, debido al mecanismo de ataque de los fagos, se ha observado que las bacterias resistentes a esos virus tienen menos capacidad para causar infecciones y enfermedades. “[Esto] las vuelve más fáciles de tratar y eliminar”, asegura Barr.
La fagoterapia ha sido objeto de muchas investigaciones y logros importantes en los últimos años. “Un estudio muy reciente determinó que, hasta la fecha, más de 2,500 pacientes han recibido la terapia con fagos; y de ellos, más de 70 por ciento mostró una mejoría importante en sus infecciones”, agrega Barr. “Los fagos pueden usarse con seguridad, y son muy eficaces en las infecciones por superbacterias”.
Este innovador tratamiento es cada vez más frecuente en algunos países. “Hace poco se administró en Escocia para tratar úlceras de pie diabético”, puntualiza Millard.
“Los estadounidenses también han utilizado la fagoterapia para casos de emergencia; y aunque todavía no se la considera un tratamiento estándar, Estados Unidos está financiando ensayos clínicos para aplicar la fagoterapia en pacientes con fibrosis quística. Por su parte, el Reino Unido tiene amplia experiencia en la investigación de bacteriófagos. De hecho, hace poco, la Universidad de Leicester creó el primer Centro para Investigación de Fagos”.

USO EN VARIOS PAÍSES
A decir del Dr. Barr, Georgia, Polonia y Rusia son los países con más amplia experiencia en tratamientos humanos con fagos, ya que algunos de sus institutos empezaron a tratar enfermos hace más de 70 años y, a la fecha, siguen utilizando la fagoterapia.
“Pese a ello, [esos países] no han investigado a fondo los mecanismos de acción de los fagos, y tampoco han llevado a cabo los ensayos clínicos requeridos”, advierte Barr. “En ese sentido, muchos otros países están impulsando los trabajos necesarios, incluidas muchas naciones europeas, Estados Unidos, Australia y China, entre otras”.
Con todo, la regulación sigue obstaculizando la implementación de la fagoterapia en otras partes del mundo. “Hacen falta muchos más fondos de investigación para asegurar que la terapia con fagos siga siendo segura y se vuelva accesible a los pacientes que la necesitan”, enfatiza el profesor de la Universidad de Monash.
“La Administración de Alimentos y Medicamentos [de Estados Unidos; FDA por sus siglas en inglés] ha planteado interrogantes en cuanto a la seguridad y la reglamentación de la fagoterapia; en consecuencia, esta alternativa terapéutica sigue considerándose experimental y no está ampliamente disponible.
“La Universidad de Monash ha creado el centro Monash Phage Foundry, donde podemos producir fagos para tratar pacientes locales con infecciones graves por superbacterias. Confío en que, en los próximos cinco años, otros países empezarán a ofrecer terapias con fagos eficaces y accesibles”, concluye el Dr. Barr. N
(Publicado en cooperación con Newsweek. Published in cooperation with Newsweek).