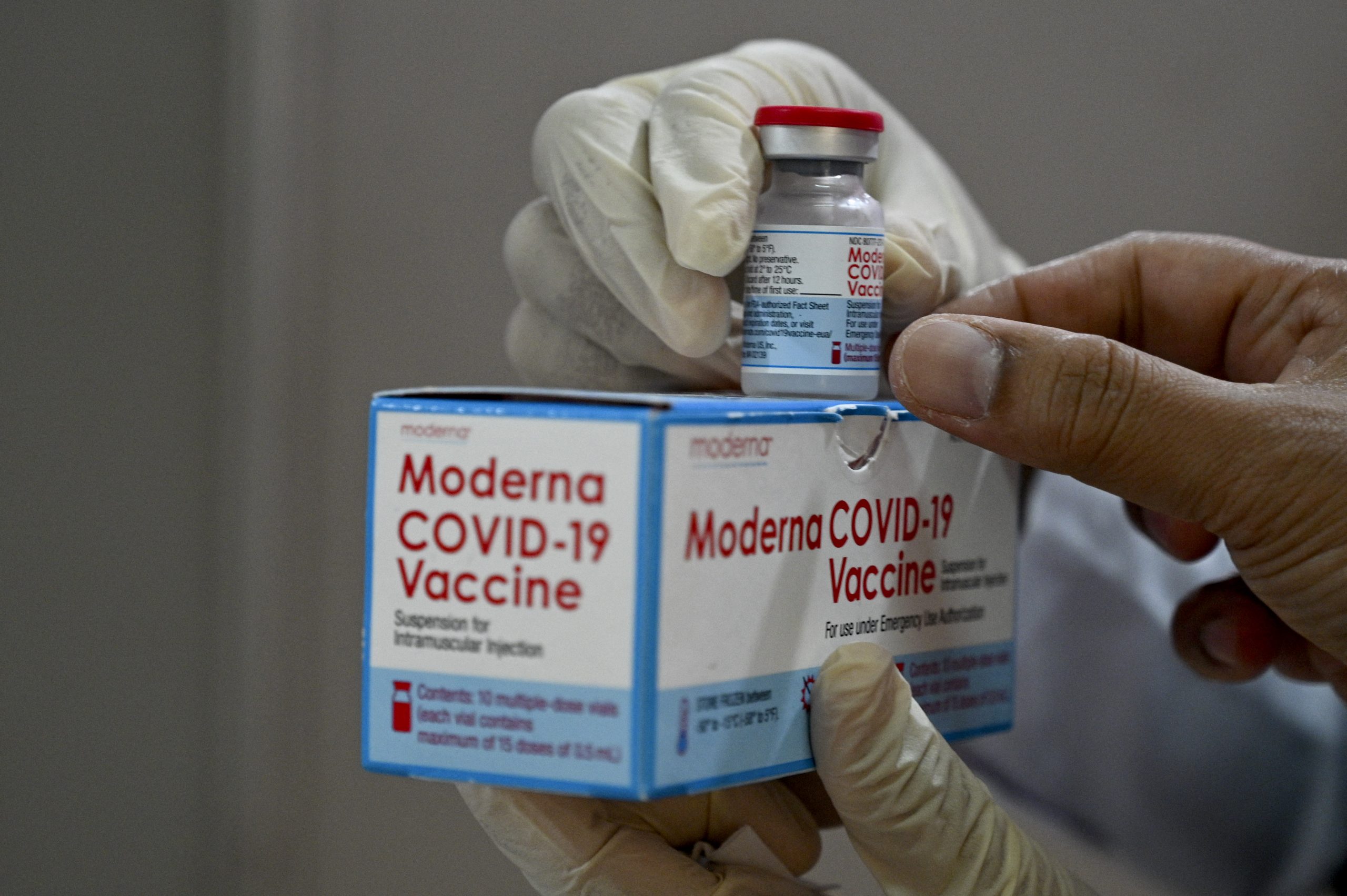
JAPÓN anuncia que dejará de usar 1,63 millones de dosis de la vacuna anticovid de Moderna, tras informes de contaminación en varios lotes.
La farmacéutica Takeda, a cargo de la venta y distribución de la vacuna de Moderna en Japón, junto con el ministerio de Salud de ese país informaron que “recibió informes de varios centros de vacunación de que sustancias ajenas fueron halladas dentro de viales cerrados en lotes específicos”.
“Tras consultas con el ministerio de Salud, hemos decidido suspender el uso de la vacuna de esos lotes a partir del 26 de agosto”, agregó.
La firma señaló que informó a Moderna y que solicitó “una investigación urgente”, en su momento Moderna no respondió a una solicitud de comentario, informó AFP.
No te pierdas: Una segunda dosis de la vacuna anticovid J&J aumenta protección: estudio
Takeda no precisó la naturaleza de la contaminación, pero indicó que no ha recibido informes de problemas de salud causados por las dosis afectadas.
El ministerio de Salud señaló que “trabajará con Takeda para obtener dosis adicionales que eviten atrasos en el programa de vacunación en Japón, que se aceleró después de un inicio lento”.
Los informes de contaminación vinieron de ocho centros de vacunación en cinco prefecturas: Aichi, Gifu, Ibaraki, Saitama y Tokio. Se confirmaron sustancias extrañas en 39 viales.
El ministerio también reveló los números de lote para que las personas afectadas puedan comprobar si pueden haber recibido una inyección potencialmente contaminada antes de que se suspendieran las dosis de la vacuna afectadas.
Actualmente cerca de 43 por ciento de la población japonesa está plenamente vacunada, pero el país enfrenta un fuerte brote de contagios provocado por la contagiosa variante delta, y varias ciudades están bajo restricciones sanitarias.
La vacuna Moderna se ha administrado principalmente en los centros de vacunación masiva y oficinas comerciales del país.
Este mismo miércoles, Moderna anunció que ha completado el proceso de presentación continua para su Solicitud de Licencia Biológica (BLA) a la Administración de Alimentos y Medicamentos (FDA) de Estados Unidos para obtener la licencia completa de su vacuna contra covid-19 para la inmunización activa para prevenir covid-19 en personas de 18 años de edad y mayores. N